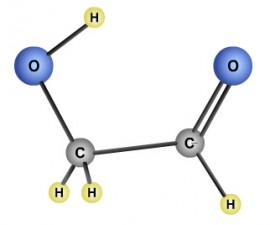
מולקולה עשויה להיות מורכבת מ:
- ממיליוני אטומים כמו מולקולת דנא
- ננוחלקיקים רבים הינם ננוגבישים, שזו פשוט מולקולה עצומה המסודרת באופן מחזורי אחיד (זה בדרך כלל לא נכון עבור הננו חלקיקים הביולוגיים)
קשרי מימן וקשרי ון דר ואלס
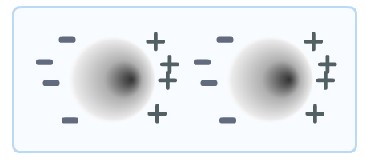
ישנם מקרים שבהם הכוחות בין האלקטרונים והגרעינים השכנים להם אינם מספיק חזקים כדי להסיט את האלקטרונים ממסלולם בצורה משמעותית, אך בכל זאת מספיקים כדי לגרום למולקולות להעדיף להיצמד אחת לשניה ללא חילופי אלקטרונים או שיתוף שלהם. כשמדובר במולקולות שבהן האלקטרונים מצטופפים יותר באזור מסוים ולכן המטען החשמלי לא אחיד (כמו למשל במולקולת מים) הקשר נקרא קשר מימן. אך אפילו מולקולות שבהן חלוקת המטענים אחידה יחסית מרגישות משיכה חלשה, וקשרים אלה נקראים קשרי ון דר ואלס.
קשרי ואן דר ואלס הם קשרים כימיים בין מולקולות ומבוססים על חלוקת המטען החשמלי בשני האטומים המשתתפים בקשר.
ההצמדות של המולקולות אינה חזקה כמו ההצמדות של אטומים בתוך מולקולות, אך היא חזקה מספיק כדי ליצור מבנים ננומטרים.
מכיוון שכוחות אלה אינם חזקים כמו כוחות מולקולרים, לא צריך גם הרבה כח בכדי להפריד בין המולקולות. בפרקים הבאים נכיר דוגמאות להשפעת כוחות אלה, כמו למשל אפקט ההדבקות של השממית לקירות, ונבין איך כוחות אלה יכולים להיות משמעותיים כשהם מצטברים, כלומר למרות שכל קשר ואן דר ואלס חלש מאד יש עדיין חשיבות לקשרים רבים אך חלשים.